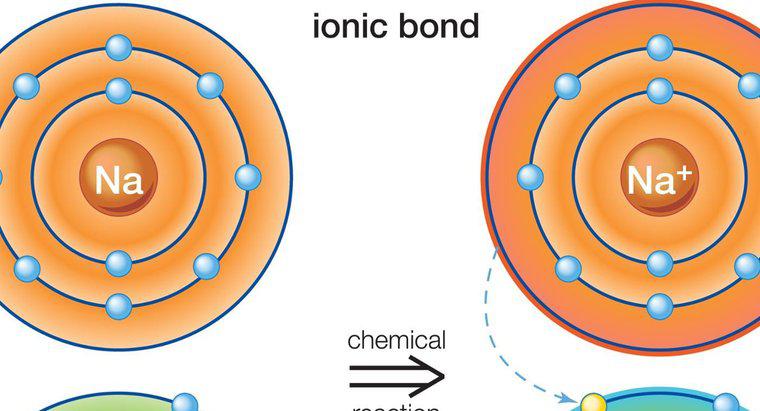
Wasserstoffbindung in lebenden Systemen ist die Bindung von Wasserstoff an ein elektronegativeres Atom. Viele organische Moleküle in Organismen, wie Proteine und Nukleinsäuren, sind für ihre korrekte Funktion auf Wasserstoffbrücken angewiesen.
Elektronegative Elemente wie Sauerstoff und Fluor neigen dazu, ihre Elektronen fest zu halten. Die Elektronegativität ist ein Maß dafür, wie stark ein Atom Elektronen anzieht. Wenn elektronegative Atome Bindungen mit anderen Atomen eingehen, ziehen sie die Elektronen stärker an. Die Elektronen verbringen mehr Zeit damit, das elektronegativere Atom zu umkreisen. Diese ungleiche Verteilung der Elektronen verursacht Bereiche mit teilweise negativen und teilweise positiven Ladungen in Verbindungen.
Wasserstoffbrücken verursachen die Spirale des DNA-Moleküls und das Faltungsmuster von Proteinen. In Proteinen ermöglichen Wasserstoffbrückenbindungen dem Protein, sich in eine dreidimensionale Struktur zu falten, die für seine Funktion wichtig ist. In der DNA werden die beiden Seiten des Moleküls durch Wasserstoffbrücken zusammengehalten.