Wasserstoffbrücken sind eine Anziehungskraft zwischen einem leicht positiven Wasserstoff eines Moleküls und einer leicht negativen Region eines anderen Moleküls. Eine einzelne Wasserstoffbrücke ist nicht sehr stark, aber in großer Zahl Wasserstoffbrücken kann eine erhebliche Anziehungskraft innerhalb einer Substanz darstellen.
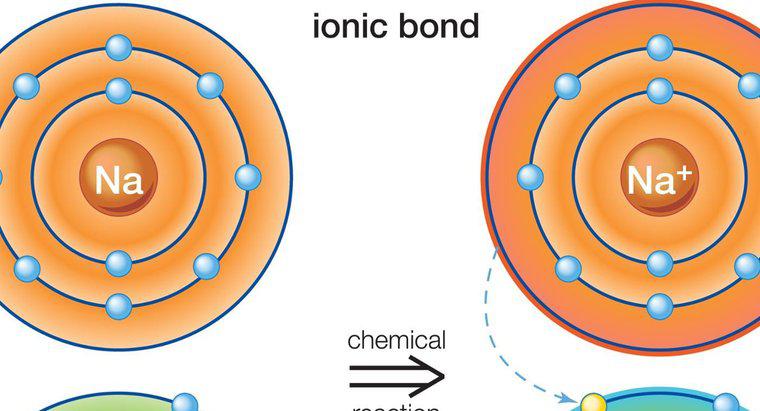
In bestimmten wasserstoffhaltigen Verbindungen werden Elektronen zwischen den Atomen der Verbindung geteilt. Einige Atome in der Verbindung ziehen die Elektronen stärker an als Wasserstoff; Daher verbringen die Elektronen mehr Zeit in der Nähe der Atome, die sie stärker anziehen. Dadurch werden die Wasserstoffbereiche eines Moleküls leicht positiv geladen und andere Bereiche leicht negativ geladen. Die leicht positiven Wasserstoffbereiche an einem Molekül ziehen die leicht negativen Bereiche an einem anderen Molekül an und bilden Wasserstoffbrücken. Verbindungen wie Wasser, die Wasserstoffbrückenbindungen enthalten, haben tendenziell höhere Siedepunkte und sind dicker oder viskoser als erwartet.