Salzsäure, deren Formel HCL (wässrig) ist, ist eine stark ätzende Säure, die hauptsächlich als Laborreagenz verwendet wird. Es ist auch eine wässrige Lösung aus Wasser und Chlorwasserstoff, einem sauren Gas.< /p>
Salzsäure ist auch als Chlorwasserstoff, Acid chlorhydrique, Chlorwasserstoffsäure, 7647-01-0, wässriger Chlorwasserstoff, Chlorwasserstoff und Muriatsäure bekannt. Es unterliegt einer exothermen Reaktion sowohl mit anorganischen Basen, zu denen Metalloxide und -hydroxide gehören, als auch mit organischen Basen, zu denen Amide und Amine gehören. Es reagiert auch mit Hydrogencarbonaten und Carbonaten zu Kohlendioxid. Seine Reaktion mit Boriden, Carbiden, Sulfiden und Phospiden erzeugt brennbare oder giftige Gase.
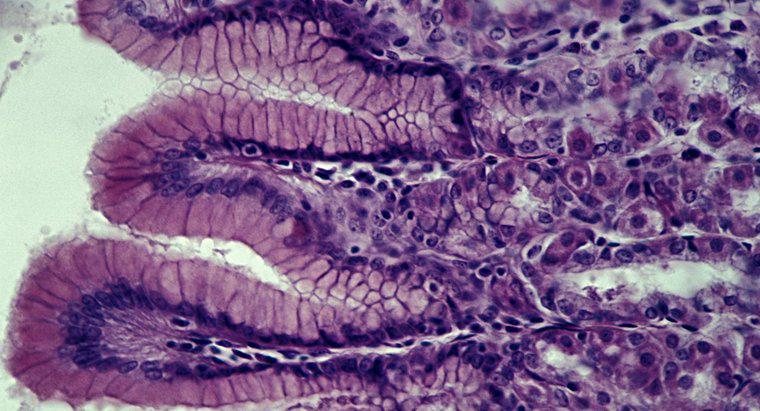
Wenn Salzsäure mit Schwefelsäure vermischt wird, bildet sich giftiges Chlorwasserstoffgas mit einer sehr gefährlichen Geschwindigkeit. Salzsäure kommt natürlicherweise sowohl im Magen vieler Säugetiere als Verdauungshilfe als auch in Gasen vor, die von Vulkanen freigesetzt werden. Beim Mischen mit Wasser dissoziiert Salzsäure unter Bildung von Hydronium- und Chloridionen, wodurch der pH-Wert des Wassers sinkt.
Wenn diese Säure in den Boden freigesetzt wird, verdunstet diese Säure von den Oberflächen von trockenem Boden, während sie in feuchtem Boden in Hydronium- und Chloridionen dissoziiert. Die Exposition gegenüber Salzsäure kann durch Inhalation oder Hautkontakt mit Produkten erfolgen, die diese Verbindungen enthalten. Es wird auch häufig in der Metallkommissionierung, Lebensmittelverarbeitung, Textil- und Gummiindustrie, Erzraffination und Herstellung von Farbstoffen und Düngemitteln verwendet.