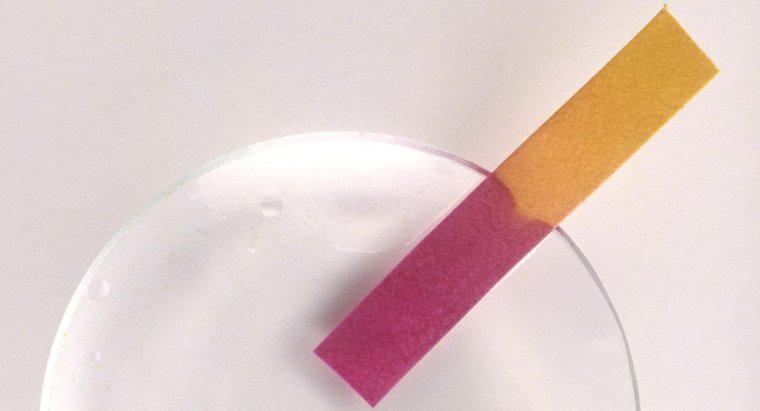Physisch gesehen haben Säuren einen säuerlichen Geschmack, sind wasserlöslich, färben blaues Lackmuspapier rot, sind ätzend, haben pH-Werte unter 7 und leiten Strom. Diese physikalischen Eigenschaften von Säuren sind ein Nebenprodukt der chemischen Eigenschaften der Säuren. Säuren können Lösungen oder reine Substanzen sein und können fester, flüssiger oder gasförmiger Natur sein.
Säuren werden als Substanzen definiert, die die Konzentration von Wasserstoffatomen oder genauer von Hydroniumatomen (H30) in Wasser erhöhen. Diese für alle Salze typische Ionisierung der Säure ist der Grund dafür, dass Säuren Strom leiten. Die pH-Werte sind als negativer Logarithmus der Konzentration von Hydroniumatomen in einer Lösung definiert; So ergeben Säuren einen pH-Wert von weniger als 7, weil die Hydroniumkonzentrationen größer als 10^-7 Mol pro Liter sind. Die Stärke einer Säure und damit ihre Korrosivität wird dadurch bestimmt, wie stark eine Säure in Wasser in Hydroniumatome ionisiert oder dissoziiert, wobei starke Säuren vollständig und schwache Säuren nur teilweise dissoziieren. Diese Hydroniumatome reagieren chemisch mit Metallen und lebendem Gewebe. Diese ätzende Eigenschaft ist im menschlichen Körper nützlich, da die Säure im Magen die Verdauung der Nahrung unterstützt. Schwache Säuren werden auch als Zusatzstoffe in Lebensmitteln verwendet, um einen sauren Geschmack zu verleihen.