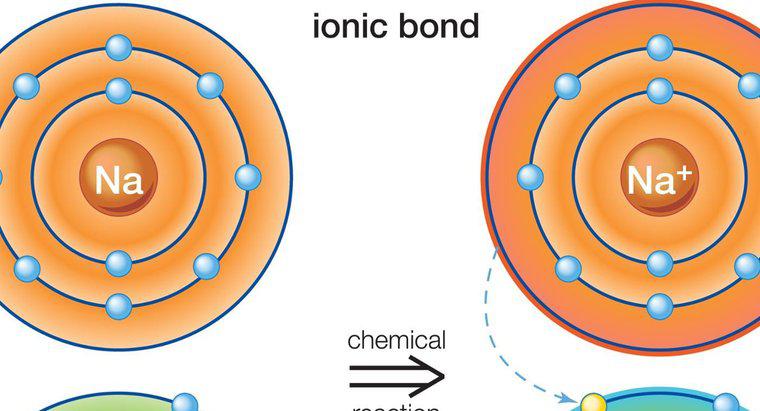
Kovalente Bindung beschreibt den Prozess, bei dem zwei Atome eine Bindung eingehen, indem sie ein oder mehrere Elektronen teilen, um ihr äußeres Orbital aufzufüllen und stabiler zu werden. Kovalente Bindungen treten typischerweise zwischen zwei Nichtmetallen auf, die sich meist auf der rechten Seite des Periodensystems befinden.
Eine kovalente Bindung kann je nach Elektronegativität der beiden beteiligten Atome entweder polar oder unpolar sein. Die Elektronegativität ist ein Maß dafür, wie stark ein Atom ein Elektron anziehen kann. Wenn die Atome, die eine kovalente Bindung bilden, unterschiedliche Elektronegativitäten haben, hat das stärkste Atom an der Bindungsstelle eine leicht negative Ladung, während das andere Atom leicht positiv ist.