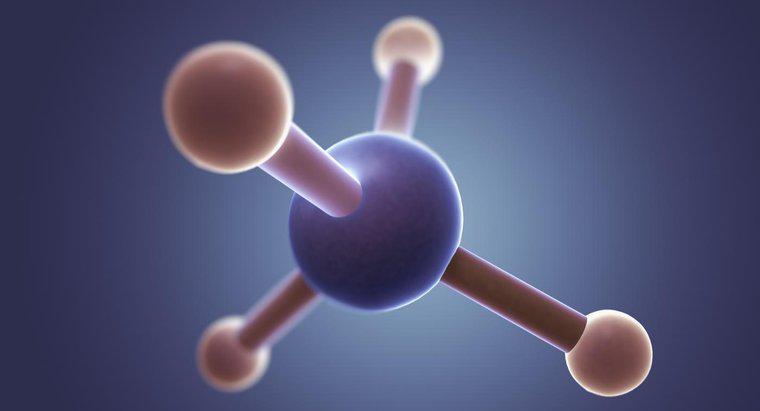
Die Lewis-Struktur von C2Cl4 umfasst eine Doppelbindungskette mit zwei Kohlenstoffatomen mit zwei Chloratomen an jedem Kohlenstoffatom. An jedem Ende sind die Chloratome ungefähr 120 Grad voneinander entfernt und vom Kohlenstoffatom.
C2Cl4 ist Tetrachlorethylen mit dem systematischen Namenssystem, aber sein gebräuchlicher Name ist Perchlorethylen. Perchlorethylen ist ein übliches chemisches Reinigungslösungsmittel. Wie seine Lewis-Struktur zeigt, ist es unpolar, was es zu einem idealen Lösungsmittel für viele andere unpolare organische Materialien macht. Die Tatsache, dass es nicht brennbar und sehr stabil ist, macht es zu einem bevorzugten Compound für den Einsatz in chemischen Reinigungen. Das Lösungsmittel wirkt auf Öle und Fette und ist daher beliebt zum Reinigen von Metallen.
C2Cl4 löst Fette im menschlichen Gewebe auf. Es entfernt die Fette von der Haut, was zu Austrocknung und Reizung führt. Es wird leicht über die Lunge aufgenommen. Die gesundheitlichen Bedenken bei C2Cl4 haben viele chemische Reinigungen dazu veranlasst, ein sichereres Lösungsmittel für ihre Anwendungen zu suchen. Die EPA stuft Tetrachlorethylen als wahrscheinlich krebserregend ein. Es ist ein Reizmittel für die Atemwege und verursacht Fortpflanzungsprobleme. Langfristiger Kontakt mit Personen, die in der chemischen Reinigung arbeiten, kann zu Problemen mit kognitiven und motorischen Fähigkeiten führen. Wenn es auf der Nordhalbkugel in die Atmosphäre freigesetzt wird, verbleibt das meiste C2Cl4 in der Luft und sein Abbau dauert bis zu 5 Monate.