Die Gesamt- oder Nettoladung jeder ionischen Verbindung muss gleich null sein. Obwohl Ionen selbst per Definition entweder positiv (Kation) oder negativ (Anion) sind, können sie sich nur so miteinander verbinden und a . bilden Verbindung besteht darin, eine entgegengesetzte Ladung zu suchen.
Eine ionische Verbindung in der Chemie bezieht sich auf jede chemische Verbindung, in der Ionen durch ionische Bindungen zusammengehalten oder gebunden werden. Ionenbindungen sind per Definition elektrostatische Anziehungen zwischen zwei Ionen mit entgegengesetzter Ladung. Mit anderen Worten, eine ionische Bindung kann sich nur zwischen einem Kation und einem Anion bilden.
Obwohl die Anzahl der in einer ionischen Verbindung enthaltenen Ionen unbegrenzt ist, muss die Nettoladung gleich Null sein, damit die Verbindung ganz bleibt. Daher muss in der fertigen Verbindung eine gleiche Anzahl von Kationen und Anionen vorhanden sein.
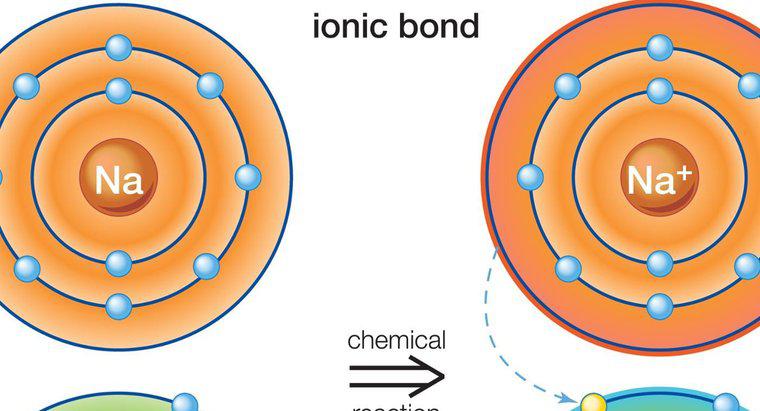
Ein beliebtes und übliches Beispiel für eine ionische Verbindung, die dieses Prinzip zeigt, ist Kochsalz oder Natriumchlorid, das die chemische Formel NaCl hat. Die Bildung von Kochsalz ist das Ergebnis einer ionischen Bindung zwischen einem Natriumkation, Na+, und einem Chloranion, Cl-. Die Struktur jedes Ions unterscheidet sich von einem Atom des gleichen Elements (Na oder Cl), das aufgrund einer gleichen Anzahl von Protonen und Elektronen eine neutrale Ladung trägt. Erst wenn jedes Atom zu einem Ion wird, kann es sich mit dem anderen Atom verbinden und eine ionische Verbindung bilden.