Moleküle werden gebildet, wenn zwei oder mehr Atome durch kovalente Bindung chemisch verbunden werden. Die Atome können aus demselben Element oder aus verschiedenen Elementen bestehen. Wenn das Molekül aus mehr als einem Element besteht, wird es als chemische Verbindung bezeichnet.
Die Eigenschaften eines Moleküls ergeben sich aus den beteiligten Elementen und den Eigenschaften der kovalenten Bindungen, die sie zusammenhalten. Kovalente Bindungen treten auf, wenn Atome Elektronen teilen, wodurch eine Bindung entsteht, die nicht leicht dissoziiert. Der Unterschied in den Elektronegativitätswerten zwischen den Atomen bestimmt die Art der gebildeten Bindung. Bei sehr ähnlichen Elektronegativitätswerten bildet sich eine unpolare kovalente Bindung. Wenn der Unterschied der Elektronegativitätswerte signifikant, aber nicht sehr unterschiedlich ist, bildet sich eine polare kovalente Bindung. Die polaren Bindungen in einem Molekül können zur Gesamtpolarität des Moleküls beitragen und ihm als polares Molekül besondere Eigenschaften verleihen.
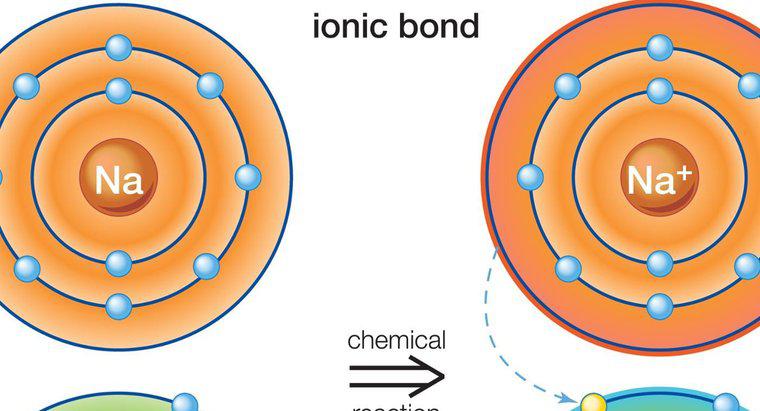
Ionische Bindungen treten auf, wenn es einen großen Unterschied in der Elektronegativität zweier Atome gibt. Ionenbindungen beinhalten die Übertragung von Elektronen von einem Atom zum anderen, um geladene Ionen zu erzeugen, die sich miteinander verbinden. Ionische Verbindungen sind keine Moleküle. Da sich kovalente Bindungen nur zwischen Nichtmetallen bilden, bestehen Moleküle nur aus nichtmetallischen Elementen.