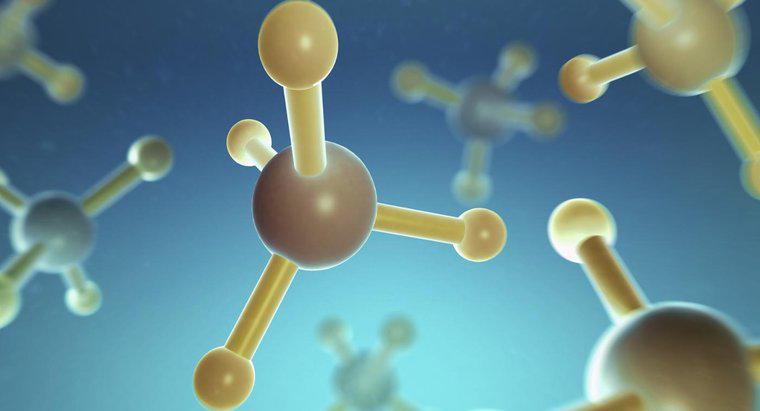
Schwefeltetrafluorid, abgekürzt als SF4, hat eine trigonal bipyramidale elektronische Geometrie. Das bedeutet, dass das zentrale Schwefelatom an vier Fluoratome gebunden ist und ein einsames Elektronenpaar besitzt.
Nach der Valenzschalen-Elektronenpaar-Abstoßungstheorie bewegen sich die Atome und das einsame Paar so weit wie möglich auseinander, was in diesem Fall eine trigonal-bipyramidale Konfiguration ergibt. Diese Struktur besteht aus einer flachen Ebene von zwei Fluoriden und einem einsamen Paar, ähnlich der Struktur eines trigonal-planaren Moleküls. Oberhalb und unterhalb der Ebene (am oberen und unteren Ende des Moleküls) befinden sich zwei weitere Fluore. Einsame Paare nehmen mehr Platz ein als Atome; daher befindet sich das einsame Paar in der Ebene, weil es dadurch am weitesten von anderen Molekülen entfernt ist.