Obwohl jedes Atom aus Teilchen unterschiedlicher Größe besteht, besteht der Großteil des Raums oder Volumens jedes Atoms aus seiner Elektronenwolke. Unter den drei vorhandenen Molekülen sind jedoch die Neutronen sind die größten und der Atomkern macht 99,9 Prozent seiner Gesamtmasse aus.
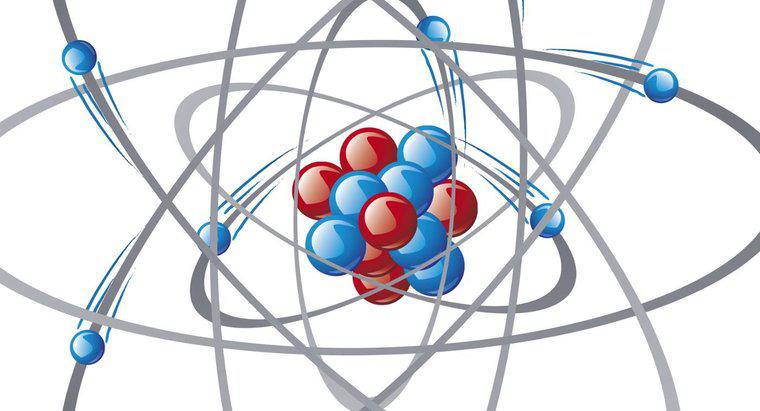
Die Grundstruktur eines jeden Atoms besteht aus einem Kern aus Protonen und Neutronen und einer Reihe winziger Elektronen, die ihn in einem Raum namens Elektronenwolke umkreisen. Die einzige Ausnahme von dieser Struktur ist das Wasserstoffatom, das keine Neutronen enthält.
Atome enthalten ebenso wie die von ihnen gebildeten Teilchen mehr Leerraum als Masse, da sich die positive Ladung der Protonen und die negative Ladung der Elektronen abstoßen. Dadurch entsteht, was Wissenschaftler eine "Elektronenwolke" nennen, die den Kern jedes Atoms umgibt. Vom Volumen her macht die Elektronenwolke den Großteil des „Raumes“ jedes Atoms aus. Eine gängige Illustration dieses Raums zeigt, dass, wenn der Kern eines Atoms die Größe einer Murmel hätte, der äußere Rand der Elektronenwolke mehr als 100 Meter oder ein Fußballfeld davon entfernt wäre.
Trotz der Tatsache, dass der größte Teil des Raums jedes Atoms seine Elektronen enthält, liegt der größte Teil seiner Masse, 99,9 Prozent, im Kern. Die Masse des Atomkerns ist fast gleichmäßig auf Protonen und Neutronen verteilt, obwohl Neutronen etwas größer sind. Die Masse eines Elektrons hingegen entspricht 1/1836 eines Protons.