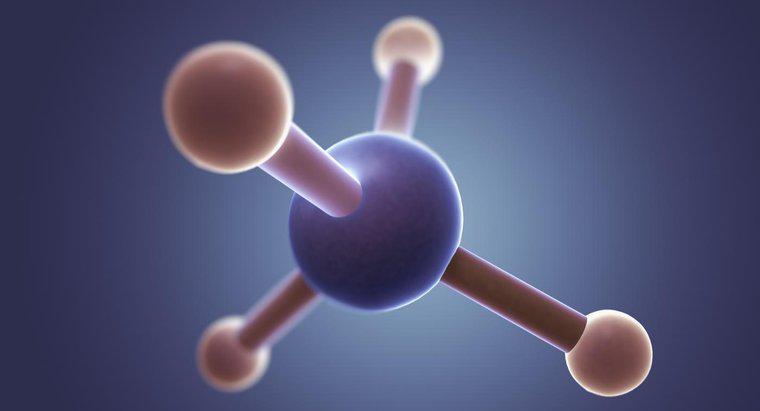
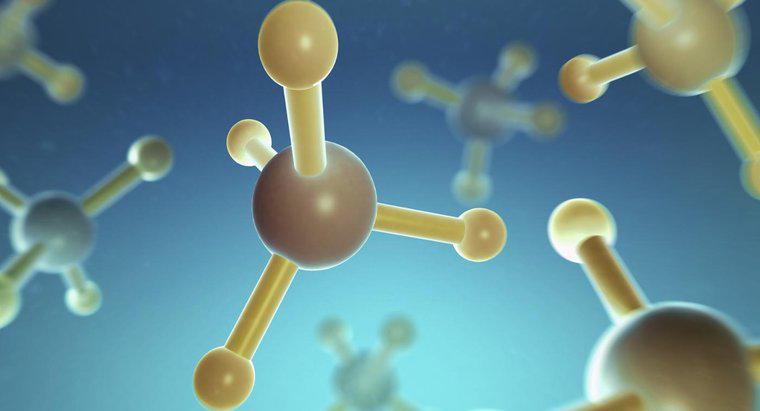
CH4 oder Methan ist ein unpolares Molekül. Methan ist ein hochsymmetrisches Molekül, das aus Atomen mit ähnlichen Elektronegativitäten besteht und folglich eine gleichmäßig verteilte Elektronenwolke und keine Bereiche mit signifikanter Ladung aufweist .
Polare Moleküle enthalten lokalisierte Bereiche positiver und negativer Ladungen. Die Polarität resultiert aus der ungleichmäßigen Verteilung der Molekülelektronenwolke. Elektronen werden ungleichmäßig verteilt, wenn Atome innerhalb des Moleküls signifikant unterschiedliche Elektronegativitätswerte aufweisen. Auch molekulare Asymmetrie kann zur Polarität beitragen. Die Kohlenstoff- und Wasserstoffatome von Methan teilen sich die Elektronen in ihren Bindungen fast zu gleichen Teilen, was zu einem nur geringen Ladungsunterschied zwischen den Kohlenstoff- und Wasserstoffatomen führt. Auch die symmetrische, tetraedrische Geometrie von Methan trägt zu seiner fehlenden Polarität bei.